Vervuilde diabetesmedicijnen in omloop
Beide media lieten vijftig tabletten van 500, 850 en 1000 milligram metformine van vijf merken analyseren op de aanwezigheid van NDMA. Uit dierproeven blijkt deze stof kankerverwekkend, reden waarom er een strenge internationale limiet is voor NDMA.
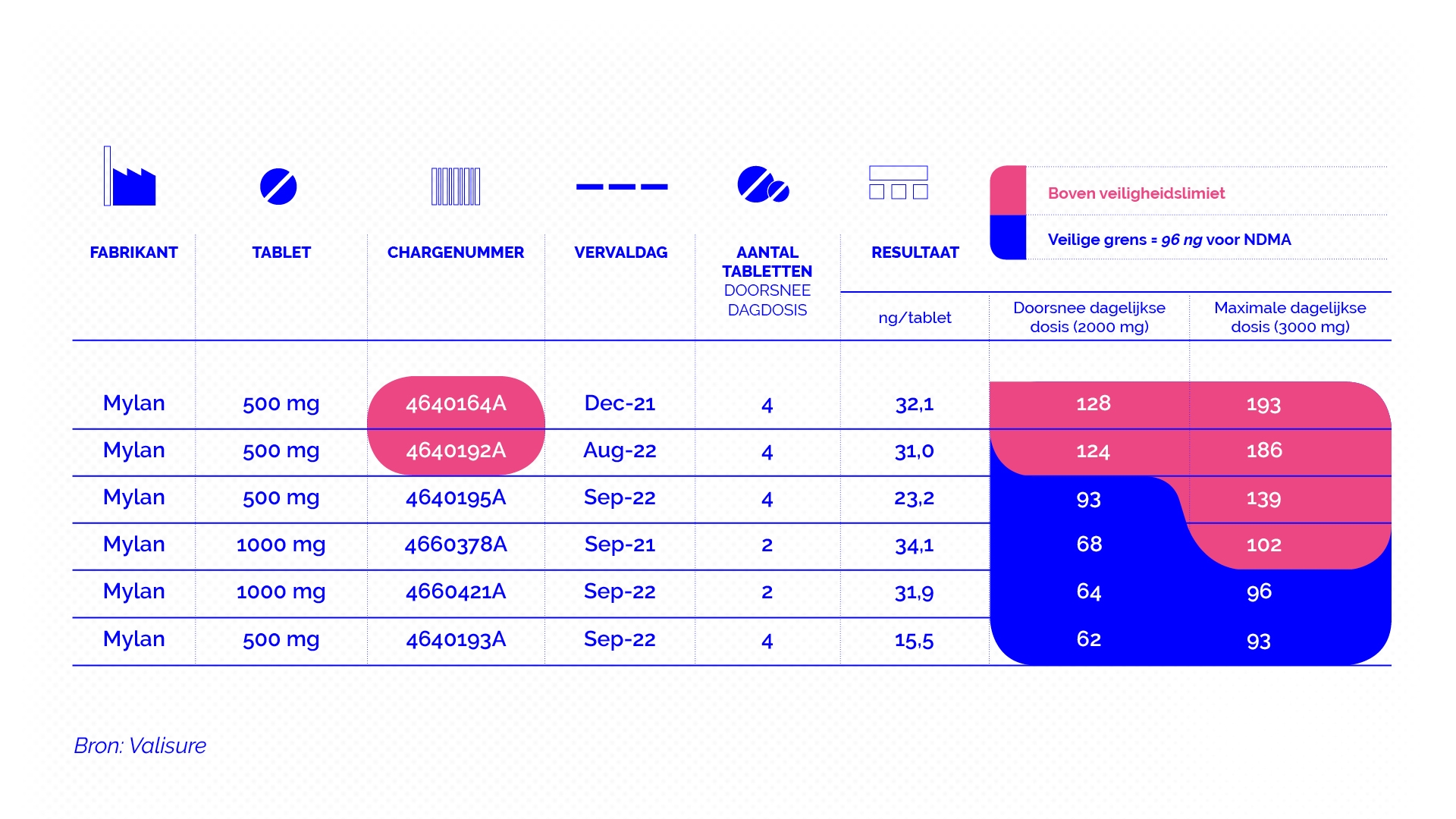
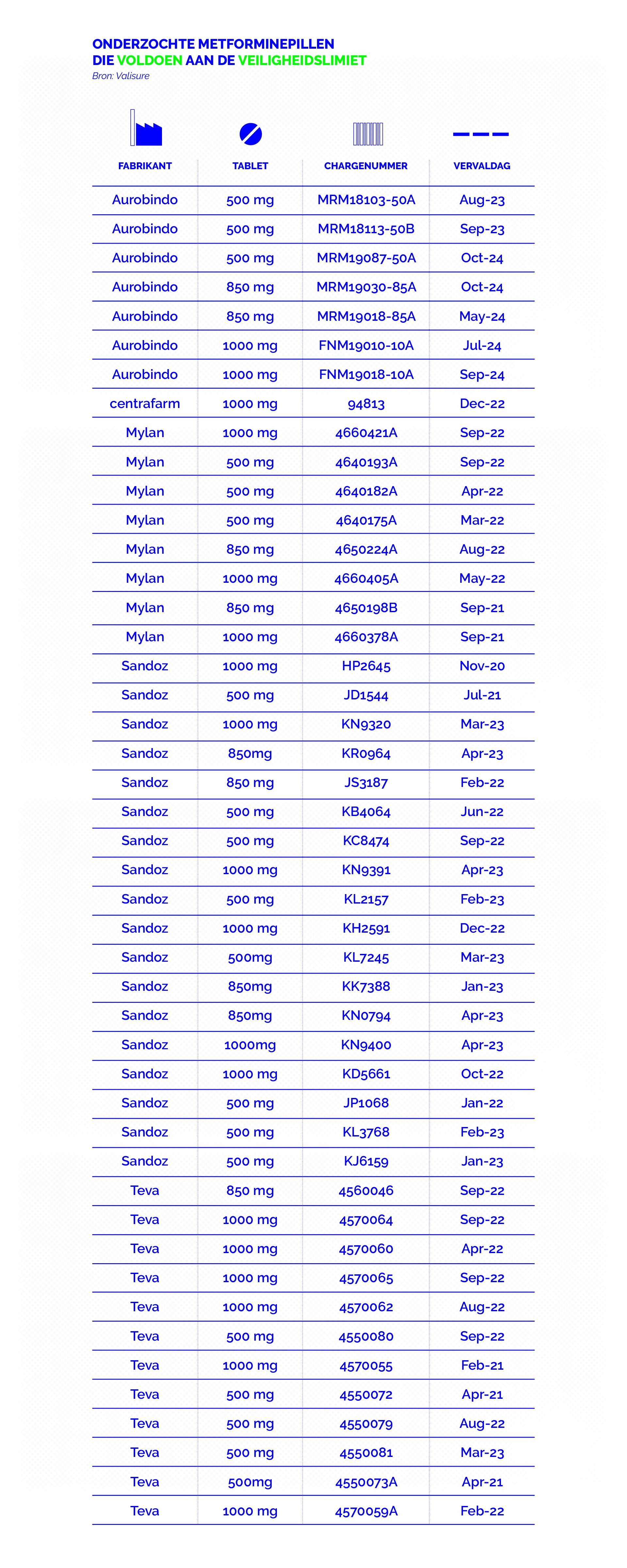
De helft van de onderzochte tabletten bevat geen traceerbare NDMA. In de andere helft verschilt de hoeveelheid, maar blijven de concentraties in de meeste gevallen onder de veiligheidslimiet. Alleen de pillen van Mylan springen er negatief uit.
Limiet
Bij een doorsnee dagdosis van 2.000 milligram metformine (vier pillen van 500 milligram) wordt bij Mylan-tabletten van twee verschillende batches de limiet overschreden. Wie deze tabletten inneemt, krijgt 128 nanogram respectievelijk 124 nanogram NDMA per dag binnen. De veiligheidslimiet is 96 nanogram NDMA per dag.
Bij de maximale dagdosis van 3.000 milligram metformine scoren vier Mylan-pillen boven de limiet, tot 193 nanogram NDMA.
Volgens IGZ en CBG roept de analyse "vragen op, maar wij kunnen op basis daarvan nog geen stappen ondernemen." Bij een terugroepactie kan een tekort aan metformine ontstaan, zeggen de toezichthouders. Voorlopig wordt patiënten geadviseerd hun metformine van Mylan te blijven gebruiken. IGZ en CBG: "We begrijpen dat de uitkomsten van het onderzoek van NRC/Zembla mogelijk onrust met zich meebrengt. De overschrijdingen die we hierin zien zijn vervelend en ongewenst, maar het gaat niet om een heel groot risico."
In Nederland gebruiken 655.000 patiënten metformine. Mylan levert een kwart van alle metformine, gebruikt bij de behandeling van diabetes type II.
Wereldwijd teruggeroepen
NDMA, voluit N-nitrosodimethylamine, behoort tot de chemische groep nitrosaminen. De stof werd in 2018 voor het eerst ontdekt in de bloeddrukverlager valsartan en nadien ook in de maagzuurremmer ranitidine. Honderden miljoenen medicijnen moesten wereldwijd worden teruggeroepen. In 2019 dook NDMA ook op in metformine.
In Europa moeten farmaceutische bedrijven vóór 15 november hun metformine testen op nitrosaminen. De testresultaten hebben de toezichthouders nodig om te beoordelen of metformine teruggeroepen moet worden.
Mylan heeft op dit moment nog niet alle resultaten ingeleverd. Het CBG heeft Mylan "dringend verzocht" de onderzoeksresultaten voor de nog niet aangeleverde batches "met spoed aan te leveren”.
Verschil
Eén van de resultaten die zijn ingeleverd door Mylan is ook getest door NRC en Zembla. Volgens Mylan zat de NDMA-waarde onder de toegestane limiet, volgens het onderzoek van NRC en Zembla zat het er boven. CBG en IGZ: "Wij gaan uitzoeken hoe dit verschil te verklaren is." Mylan zegt desgevraagd dat tot nu toe "geen kwantificeerbare niveaus van NDMA geïdentificeerd" zijn "voor tot dusver geteste batches die in Nederland zijn verspreid."
Door: Annette Schätzle, Jos van Dongen en Joep Dohmen
Over dit onderzoek
NRC en Zembla hebben vijftig pillen van het diabetes type 2 medicijn metformine laten onderzoeken door Valisure. Deze apotheek uit New Haven in de Amerikaanse Staat Connecticut heeft een gecertificeerd laboratorium waarin begin van dit jaar op grote schaal metforminepillen zijn getest.
Toen trof Valisure ook in Amerikaanse diabetes type 2 tabletten te hoge concentraties van de kankerverwekkende stof NDMA aan. Valisure heeft deze testresultaten op 2 maart met de Amerikaanse toezichthouder FDA gedeeld.
In juli publiceerde de FDA een artikel waarin de ontoelaatbare overschrijdingen van de kankerverwekkende stof in metformine bevestigd wordt. De FDA constateert ook tekortkomingen in de meetmethode van Valisure. Valisure heeft zijn methodiek inmiddels hierop aangepast.
De pillen in dit onderzoek naar Nederlandse metforminepillen zijn volgens deze aangepaste testwijze geanalyseerd. Valisure publiceert deze week een verantwoording van hun onderzoeksmethode op hun website: www.valisure.com.
- Mylan
Praat mee
Altijd op de hoogte blijven van het laatste nieuws?
Schrijf je in voor de Zembla-nieuwsbrief en blijf op de hoogte van onze onthullende journalistiek.