Snelle goedkeuring van coronavaccins verwacht na aanleveren kwaliteit
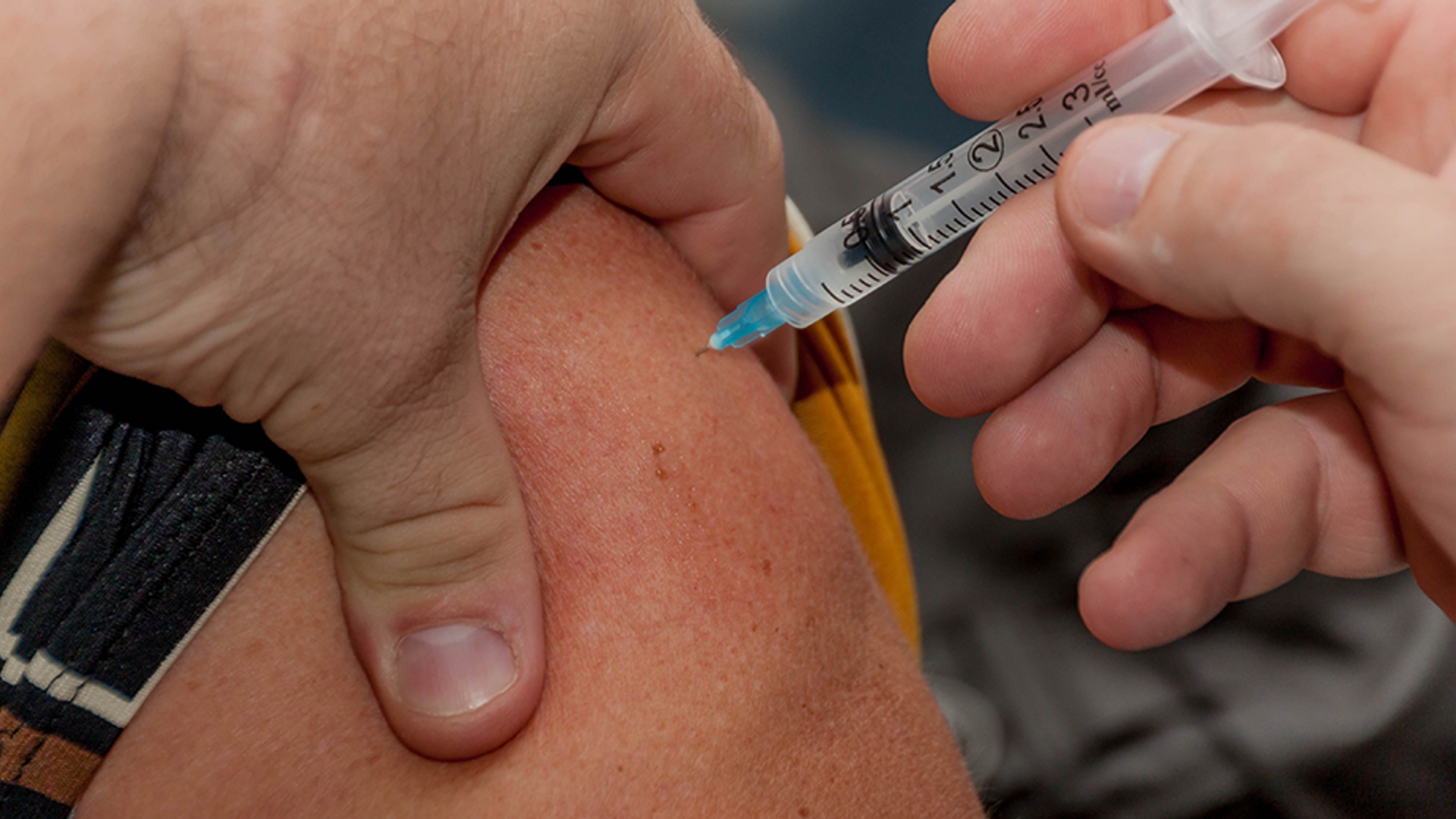
De goedkeuring van coronavaccins kan in korte tijd worden afgerond, indien de ontwikkelaars wel onderzoeksresultaten van hoge kwaliteit aanleveren. "Als alles perfect is en de aanvraag geen vragen oproept, kan het heel snel gaan", stelt een woordvoerster van het College ter Beoordeling van Geneesmiddelen (CBG). Samen met de andere medicijnautoriteiten uit EU-landen moet het CBG uiteindelijk een oordeel vellen over de toelating van vaccins.
Wetenschappers van nationale medicijnautoriteiten zitten samen in het Europese Geneesmiddelenbeoordelingscomité CHMP van het Europees Medicijnagentschap in Amsterdam. Zij wachten nog op de definitieve onderzoeksresultaten uit de derde en laatste onderzoeksfase. "De bal ligt bij de firma's. Wij wachten op hun data, die zullen ze waarschijnlijk snel aanleveren", aldus de woordvoerster van het CBG.
Oxfordvaccin voor 90 procent effectief
Vorige week maakten de farmaceutische bedrijven Moderna en Pfizer/BioNTech veelbelovende resultaten bekend uit de derde fase van hun onderzoeken. AstraZeneca, dat samen met de Universiteit van Oxford een vaccin heeft ontwikkeld, voegde zich maandag bij de concurrenten. Het 'Oxfordvaccin' blijkt voor 90 procent effectief, wanneer mensen eerst een halve dosis krijgen en met een tweede prik op een later moment een volledige dosis. Zowel Moderna als Pfizer/BioNTech hebben een effectiviteit van rond de 95 procent gerapporteerd.
Beoordeling drie vaccins: kwaliteit, veiligheid en effectiviteit
De beoordeling van de genoemde drie vaccins is in Europa al in oktober begonnen. Om tijd te besparen begon het CHMP al aan de evaluatie van de eerste twee onderzoeksfases, terwijl de derde fase nog gaande was. Dat heet in vaktermen een rolling review.
EMA en CBG benadrukken dat de gebruikelijke strenge eisen gelden als altijd qua kwaliteit, veiligheid en effectiviteit. "Hoewel de nood voor een vaccin hoog is, blijft het belangrijk dat we het proces van beoordeling nauwkeurig uitvoeren. Daarbij staat veiligheid bovenaan", aldus het CBG.
Vervolgstappen vaccins
Als de wetenschappers van het CHMP groen licht geven voor een vaccin, gaat de aanvraag naar de Europese Commissie, die het uiteindelijke besluit neemt over toelating tot de Europese markt. Commissievoorzitter Ursula von der Leyen zei vorige week dat over de vaccins van Pfizer en Moderna mogelijk al in de tweede helft van december een besluit kan vallen.
Binnen het Europese beoordelingscomité mogen experts uit alle EU-landen commentaar geven op de onderzoeksresultaten. Daarna beslissen ze samen over het te geven advies. Twee lidstaten spelen hierin een 'voortrekkersrol'. Wetenschappers uit die landen coördineren de beoordeling. Wie dat zijn, wordt pas bekendgemaakt nadat het besluit is gevallen, legt de woordvoerster van het CBG uit. ANP
Praat mee
Altijd op de hoogte blijven van het laatste nieuws?
Meld je snel en gratis aan voor de Kassa nieuwsbrief!
